Das pilozytische Astrozytom (Grad 1) kommt meist bei Kindern und jungen Erwachsenen vor. Das pilozytische Astrozytom ist der häufigste Gehirntumor des Kindesalters.
Betroffen sind hauptsächlich
- das Kleinhirn,
- die Basalganglien,
- der Thalamus,
- der Hirnstamm und
- der Sehnerv (Nervus opticus; sog. Optikusgliom).
Der Hirntumor Grad 1 wächst nur langsam und ist hinsichtlich seiner Wachstumseigenschaften deutlich vom umliegenden Hirngewebe abgegrenzt. Er verläuft in 99 Prozent der Fälle gutartig und ist bei vollständiger operativer Entfernung heilbar.
Vom diffusen Astrozytom (Grad 2) sind meist Personen des mittleren Lebensalters (30. bis 40. Lebensjahr) betroffen. Er befindet sich in den meisten Fällen in der weißen Substanz des Großhirns, häufig im Bereich des Stirnlappens. Auch im Thalamus, Mittelhirn und Brücke ist das diffuse Astrozytom oft zu finden. Seltener tritt dieser Tumor im Schläfen- oder Scheitellappen auf.
Das Grad-2-Astrozytom wächst sehr langsam. Es beeinträchtigt dabei aber auch gesundes Gewebe in seinem Umfeld ("diffuses Wachstum"). In etwa 10 Prozent der Fälle pro Jahr kommt es unbehandelt zu einer bösartigen Entartung.
Ein anaplastisches Astrozytom (Grad 3) kommt bei Menschen vor, die zwischen 35 und 45 Jahre alt sind. Der Tumor vergrößert sich schneller als beim Grad 2. Er ist im Großhirn lokalisiert und kann sich ebenfalls zum Glioblastom weiterentwickeln.
Das Glioblastom (Grad 4) kommt in der Regel bei Menschen nach dem 50. Lebensjahr vor. Es ist das bösartigste und mit 3 Neuerkrankungen auf 100.000 Personen das häufigste Gliom.
Der Tumor geht hauptsächlich von der weißen Substanz des Großhirns aus. Er wächst infiltrierend, das heißt in das gesunde Hirngewebe hinein.
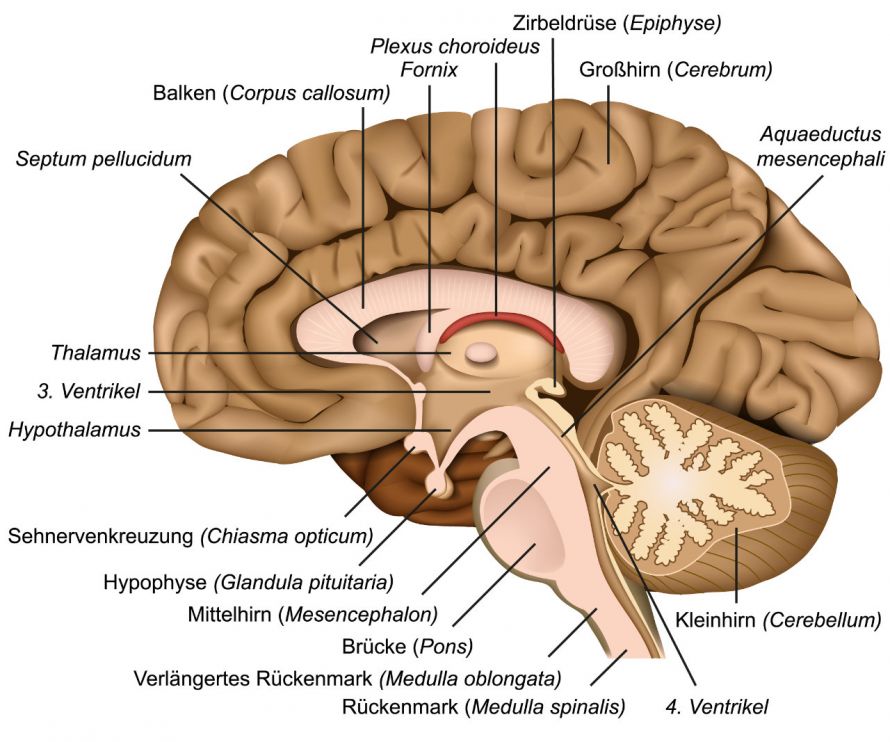
Ein Astrozytom kann verschiedene Bereiche des Gehirns betreffen © bilderzwerg | AdobeStock
Grundsätzlich entwickelt das Astrozytom ähnliche Symptome wie andere Hirntumoren. Die genauen Symptome hängen aber vor allem von der Lokalisierung des Tumors ab.
In der Nähe der Sehbahn befindliche Astrozytome beeinträchtigen das Sehvermögen. Es kommt zu einem Hervortreten des Augapfels (sog. Exophthalmus).
Wächst der Tumor im Kleinhirn, leidet der Patient an
- Zittern der Hände,
- gestörtem Koordinationsvermögen der Gliedmaßen und
- anderen von dieser Gehirnregion gesteuerten Funktionen.
Weitere mögliche Symptome eines Gehirntumors sind
Die Tumorart bildet sich aus den Astrozyten. Dieser Zelltyp gehört zur Gruppe der Stützzellen (Gliazellen) im Gehirn. Stützzellen sind für die Abgrenzung der Nervenzellen von den Blutgefäßen und der Oberfläche des Gehirns zuständig.
Astrozytome entstehen durch genetische Veränderungen, die eine Störung der Wachstumskontrolle von Astrozyten zur Folge haben. Dadurch kommt es zu ungehemmten Zellteilungen und zur Entstehung eines Tumors.
Als Ursachen für solche genetischen Veränderungen werden verschiedene Faktoren diskutiert. Als gesichert gilt, dass sich Hirntumoren als Folge einer Strahlentherapie entwickeln können.
Die Medizin geht aber davon aus, dass das Astrozytom meist nicht erblich bedingt ist. Allerdings gibt es bestimmte genetisch bedingte Erkrankungen, bei denen Astrozytome gehäuft auftreten. Das ist z.B. die Neurofibromatose vom Typ 1 und 2 (eine seltene Hauterkrankung).
Die wichtigste Untersuchungsmethode bei Verdacht auf ein Astrozytom ist die Magnetresonanztomographie (MRT, auch Kernspintomographie genannt, Abb.1). Mithilfe eines Kontrastmittels erkennen Neurologen das Astrozytom als entweder gut abgegrenzten oder diffusen Bereich im Kernspintomogramm.
Bei einem Astrozytom Grad 1 leuchtet die betroffene Hirnregion deutlich auf, da der Tumor scharf begrenzt ist.
Tumoren der Grade 2 und 3 sind nur als mehr oder weniger dunkle Areale zu erkennen. Das Glioblastom ist als ringförmiges Gebilde zu sehen.

Abb. 1: MRT-Bild eines Astrozytoms. Im Tumor-Bild ist es heller als das normale Gehirn. Der Tumorgrad WHO II oder WHO III und das molekulare Profil als Astrozytom sind nicht auf dem MRT zu erkennen. Mit speziellen metabolischen Sequenzen oder einer PET-Untersuchung ist das teilweise möglich. Erst die Untersuchung von entnommenen Gewebe (Biopsie) bringt die Diagnose der molekularen Eigenschaften und Methylierungsmerkmale des Tumors. [Quelle: Prof. Dr. Andreas Raabe; Inselspital Bern]
Zur Sicherung der Diagnose dient oft eine Biopsie. Dabei entnimmt der Neurochirurg operativ eine Gewebeprobe aus der betroffenen Hirnregion. Diese Probe wird im Labor auf bösartige Zellen untersucht. Das Ergebnis dieser feingeweblichen (histologischen) Untersuchung ist wichtig: Damit bestimmen die Mediziner den Grad der Bösartigkeit des Tumors und planen daraufhin die Therapie.
In ausgewählten Fällen wird auf das Vorhandensein bestimmter molekularer Marker hin untersucht. Deren Präsenz bzw. Fehlen kann einen Einfluss auf die Prognose und die Therapieentscheidung haben.
Eine weitere Untersuchungsmethode ist die Liquor-Diagnostik. Darunter versteht man die Entnahme und Untersuchung von Flüssigkeit aus dem Rückenmark. Sie spielt insbesondere bei der Abgrenzung zu anderen Krankheiten eine Rolle.
Bei der Therapieentscheidung muss der behandelnde Arzt Risiken und Nutzen abwägen. Er bezieht
- das Alter des Patienten,
- den Allgemeinzustand und
- den neurologischen Zustand
in die Therapieplanung mit ein.
Neben diesen nicht-beeinflussbaren Faktoren gibt es noch beeinflussbare Faktoren. Auch sie bestimmen den Erfolg einer Behandlung. Dazu gehören u. a.
- die Zeit bis zur Operation (je kürzer, desto besser),
- das Ausmaß der Tumorresektion (Verkleinerung vs. Komplette Tumorresektion) sowie
- die Aufnahme einer Chemotherapie / Bestrahlung bei inoperablen Astrozytomen.
Grundsätzlich stehen als therapeutische Möglichkeiten beim Astrozytom somit
- eine Operation,
- eine Strahlentherapie und
- eine Chemotherapie
zur Verfügung.
Die moderne Strategie der sehr zeitigen Operation des Astrozytoms beruht auf relativ neuen Beobachtungen. Eine Studie verglich die Überlebenszeiten von Patienten aus zwei Universitäten mit zwei unterschiedlichen, aber konsequent verfolgten Strategien. Sie wies einen klaren Überlebensvorteil für operierte Patienten nach.
Die Verlaufsbeobachtung über Jahre hinweg oder eine alleinige Biopsie und Chemotherapie bzw. Bestrahlung ohne Operation führten hingegen häufiger zur malignen Entartung und einem damit einhergehenden beschleunigten Krankheitsverlauf.
Beim pilozytischen Astrozytom (WHO-Grad 1) reicht meist der operative Eingriff aus. Befindet sich der Tumor im Kleinhirn, lässt er sich in den meisten Fällen vollständig entfernen. Das ergibt dann eine sehr gute Prognose und die Symptome bessern sich rasch.
Pilozytische Astrozytome
- in den Basalganglien,
- im Thalamus und
- im Hirnstamm
werden mit mikrochirurgischen Methoden entfernt. Eine komplette Entfernung ist aber häufig nicht möglich, sodass sich in der Regel eine Strahlentherapie anschließt.
Insbesondere kleinere diffuse Astrozytome (WHO-Grad 2) können operativ entfernt werden. Abhängig vom Ergebnis der feingeweblichen Untersuchung wird dann
- entweder abgewartet, ob sich nach der Hirntumor-Operation ein erneutes Tumorwachstum einstellt, oder
- es wird mit einer Bestrahlung begonnen.
Ziel einer Operation ist normalerweise die vollständige Entfernung des Tumorgewebes. Der Tumor wächst aber auch in gesundes Gehirngewebe hinein. Daher besteht die Gefahr von neurologischen Ausfällen, wenn auch gesundes Gehirngewebe mit dem Tumorgewebe entfernt wird. Deshalb können größere Tumoren in der Regel nicht vollständig entfernt werden.
In diesen Fällen ist die Strahlentherapie von Bedeutung.
Nur bei sehr ausgedehnten Tumoren und bei erneutem Tumorwachstum nach einer Strahlentherapie erfolgt eine Chemotherapie.
Auch das anaplastische Astrozytom (WHO-Grad 3) wächst in gesundes Gewebe hinein. Daher ist eine komplette operative Entfernung wie bei den anderen Gliomen nicht möglich.
Das Ziel der Operation besteht vielmehr darin, die Größe des Tumors zu reduzieren. Das erhöht die Erfolgsaussichten der anschließenden Strahlenbehandlung oder der Chemotherapie.
Nach Diagnose eines Astrozytoms erfolgt in der Regel lebenslang eine Verlaufskontrolle mittels MRT. Dabei wird das Intervall der Bildgebung jedoch inpiduell angepasst. Als Standard gelten derzeit die folgenden Zeiten:
- alle 3 Monate: nach der Operation, bei WHO-Grad III, bei sichtbaren Tumorresten, bei IDH-Wildtyp-Tumoren sowie bei PET-aktiven Tumorresten,
- alle 3-12 Monate: je nach Tumorart, molekularem Profil, Resektionsgrad und vorheriger Zeit der Tumorfreiheit bzw. progressionsfreiem Intervall.
Die meisten Patienten sollten nach dem Berner OPTIMISST-Protokoll bereits am Tag nach der Operation schnell wieder aktiv werden.
Patienten mit größeren Tumoren oder komplizierter Lage sollten etwa ein bis zwei Monate zur Erholung nach der Operation einplanen. Hier gilt es, innerhalb der Familie und mit dem Arbeitgeber optimale und stressfreie Verhältnisse für die Operation zu schaffen.
Bei besonders schwierigen Operationen sind Defizite zu erwarten. In 95 % der Fälle sind diese Defizite aber vorrübergehend. Dann ist eine konzentrierte Neurorehabilitation einzuplanen. Spätestens eine Woche nach der Operation liegt zudem die Gewebediagnose vor. Nach einer weiteren Woche folgt die molekulare Diagnose. Danach planen die Mediziner im Tumorboard das weitere Vorgehen.
Der festgestellte Grad des Tumors hat einen großen Einfluss auf den weiteren Verlauf des Lebens und der Erkrankung.
Astrozytome des Grades 1 haben eine günstige Prognose. Fünf Jahre nach der Diagnose des Tumors lebten noch 9 von 10 Patienten. Die meisten Patienten gelten zudem nach dem operativen Eingriff als „geheilt“, wenn der Tumor komplett entfernt werden kann.
Bei Patienten mit Tumoren vom Grad 2 ist oft nach 2-8 Jahren eine weitere Operation notwendig. Bei kleinen Tumoren und günstigen Tumoreigenschaften kann eine Operation mehr als 99,99% der Tumorzellen entfernen. Dann bleiben nur wenige Zellen übrig, und nicht alle diese Zellen wachsen danach wieder.
Daher gibt es Patienten, bei denen der Tumor sich über Jahrzehnte und zu Lebzeiten nicht wieder ausbildet. Man spricht daher richtigerweise eher von einer „Langzeit-Kontrolle“ als von Heilung.
Beim Grad 3 wächst das Tumorgewebe rascher nach. Je nach den genauen Zelleigenschaften ist aber auch Tumorfreiheit über mehrere Jahre möglich. Die Lebenserwartung bei Patienten mit Astrozytom Grad 3 ist sehr viel geringer als die bei Patienten mit Astrozytom Grad 1.
Die ungünstigste Prognose hat allerdings das Astrozytom Grad 4 (“Glioblastom“): Fünf Jahre nach der Diagnose lebten nur noch 5 von 100 Patienten. Allerdings können mithilfe moderner Chemotherapien die Überlebenszeiten insbesondere bei jüngeren Patienten verlängert werden.






















